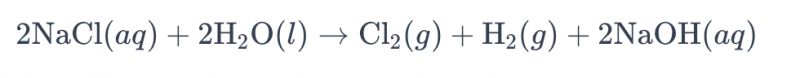تُعرف عملية التحليل الكهربائي لمحلول ملحي باستخدام أقطاب التيتانيوم لإنتاج الكلور باسم "التحليل الكهربائي للمحلول الملحي". في هذه العملية، تُستخدم أقطاب التيتانيوم لتسهيل تفاعل أكسدة أيونات الكلوريد في المحلول الملحي، مما يؤدي إلى توليد غاز الكلور. المعادلة الكيميائية العامة للتفاعل هي كما يلي:
في هذه المعادلة، تتأكسد أيونات الكلوريد عند المصعد، مما ينتج عنه غاز الكلور، بينما تختزل جزيئات الماء عند المهبط، مما ينتج عنه غاز الهيدروجين. بالإضافة إلى ذلك، تختزل أيونات الهيدروكسيد عند المصعد، مكونة غاز الهيدروجين وهيدروكسيد الصوديوم.
يعود اختيار أقطاب التيتانيوم إلى مقاومتها الممتازة للتآكل وتوصيلها الكهربائي العالي، مما يسمح لها بالخضوع للتفاعل بثبات أثناء التحليل الكهربائي دون تآكل. وهذا ما يجعل أقطاب التيتانيوم خيارًا مثاليًا لتحليل المحلول الملحي كهربائيًا.
تتطلب عملية التحليل الكهربائي للمياه المالحة عادةً مصدر طاقة خارجي لتوفير الطاقة اللازمة للتفاعل. ويكون هذا المصدر عادةً عبارة عن مصدر تيار مستمر، لأن التفاعلات الكهربائية تتطلب اتجاهًا ثابتًا لتدفق التيار، ويمكن لمصدر التيار المستمر توفير هذا الاتجاه.
في عملية التحليل الكهربائي للمياه المالحة لإنتاج غاز الكلور، يُستخدم عادةً مصدر طاقة تيار مستمر منخفض الجهد. يعتمد جهد مصدر الطاقة على ظروف التفاعل المحددة وتصميم الجهاز، ولكنه يتراوح عمومًا بين 2 و4 فولت. بالإضافة إلى ذلك، تُعد شدة التيار الكهربائي لمصدر الطاقة عاملًا حاسمًا يجب تحديده بناءً على حجم حجرة التفاعل والإنتاجية المطلوبة.
باختصار، يعتمد اختيار مصدر الطاقة لتحليل المياه المالحة كهربائياً على المتطلبات المحددة للتجارب أو العمليات الصناعية لضمان التفاعل الفعال والحصول على المنتجات المطلوبة.
تاريخ النشر: 16 يناير 2024